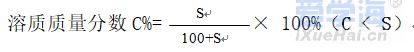【初中化学】人教版九年级下册 第九单元 溶液
 2022-01-10
2022-01-10 
 iXueHai.cn
iXueHai.cn
 爱学海
字体 - 小
+ 大 纠错指正
爱学海
字体 - 小
+ 大 纠错指正
|
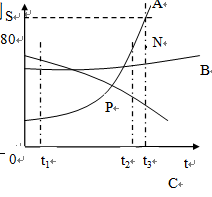
第九单元 溶液 课题1 溶液的形成 1、溶液 (1)溶液的概念:一种或几种物质分散到另一种物质里形成的均一的、稳定的混合物,叫做溶液 (2)溶液的基本特征:均一性、稳定性注意: a、溶液不一定无色,如CuSO4为蓝色 FeSO4为浅绿色 Fe2(SO4)3溶液为黄色 b、溶质可以是固体、液体或气体;水是最常用的溶剂 c、溶液的质量 = 溶质的质量 + 溶剂的质量 溶液的体积 ≠ 溶质的体积 + 溶剂的体积 d、溶液的名称:溶质的溶剂溶液(如:碘酒——碘的酒精溶液) 2、溶质和溶剂的判断 3、饱和溶液、不饱和溶液(1)概念: (2)判断方法:继续加入该溶质,看能否溶解 (3)饱和溶液和不饱和溶液之间的转化  注:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低 ②最可靠的方法是:加溶质、蒸发溶剂 (4)浓、稀溶液与饱和不饱和溶液之间的关系 ①饱和溶液不一定是浓溶液 ②不饱和溶液不一定是稀溶液,如饱和的石灰水溶液就是稀溶液 ③在一定温度时,同一种溶质的饱和溶液要比它的不饱和溶液浓 (5)溶解时放热、吸热现象 溶解吸热:如NH4NO3溶解 溶解放热:如NaOH溶解、浓H2SO4溶解溶解没有明显热现象:如NaCl 课题2 溶解度 1、固体的溶解度 (1)溶解度的定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量四要素: ①条件:一定温度 ②标准:100g溶剂 ③状态:达到饱和 ④质量:溶解度的单位:克 (2)溶解度的含义: 20℃时NaCl的溶液度为36g含义:在20℃时,在100克水中最多能溶解36克NaCl,或在20℃时,NaCl在100克水中达到饱和状态时所溶解的质量为36克 (3)影响固体溶解度的因素: ①溶质、溶剂的性质(种类) ②温度 a、大多数固体物的溶解度随温度升高而升高;如KNO3 b、少数固体物质的溶解度受温度的影响很小;如NaCl c、极少数物质溶解度随温度升高而降低。如Ca(OH)2 (4)溶解度曲线 例: (1)t3℃时A的溶解度为 80g; (2)P点的的含义 在该温度时,A和C的溶解度相同; (3)N点为 t3℃时A的不饱和溶液 ,可通过 加入A物质降温, 蒸发溶剂 的方法使它变为饱和; (4)t1℃时A、B、C、溶解度由大到小的顺序C>B>A (5)从A溶液中获取A晶体可用降温结晶的方法获取晶体。 (6)从B的溶液中获取晶体,适宜采用 蒸发结晶的方法获取晶体 (7)t2℃ 时A、B、C的饱和溶液各W克,降温到t1℃会析出晶体的有A和B无晶体析出的有C,所得溶液中溶质的质量分数由小到大依次为 A<C<B (8)除去A中的泥沙用 过滤 法;分离A与B(含量少)的混合物,用 结晶 法。 2、气体的溶解度 (1)气体溶解度的定义:在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。 (2)影响因素: ①气体的性质 ②温度(温度越高,气体溶解度越小) ③压强(压强越大,气体溶解度越大) 3、混合物的分离 (1)过滤法:分离可溶物 + 难溶物 (2)结晶法:分离几种可溶性物质 结晶的两种方法 (1)蒸发溶剂,如NaCl(海水晒盐) (2)降低温度(冷却热的饱和溶液,如KNO3) 课题3 溶液的浓度 1、公式: 2、在饱和溶液中 3、配制一定溶质质量分数的溶液 (1)用固体配制: ①步骤:计算、称量、溶解 ②仪器:天平、药匙、量筒、滴管、烧杯、玻璃棒 (2)用浓溶液稀释(稀释前后,溶质的质量不变) ①步骤:计算、量取、稀释 ②仪器:量筒、滴管、烧杯、玻璃棒 |
| 高三: 语文| 数学| 英语| 物理| 化学| 地理| 生物| 历史| 思想政治| 信息技术| 初三: 语文| 数学| 英语| 物理| 化学| 历史| 道德与法制 |
| 高二: 语文| 数学| 英语| 物理| 化学| 地理| 生物| 历史| 思想政治| 信息技术| 初二: 语文| 数学| 英语| 物理| 地理| 生物| 历史| 道法 |
| 高一: 语文| 数学| 英语| 物理| 化学| 地理| 生物| 历史| 思想政治| 信息技术| 初一: 语文| 数学| 英语| 物理| 地理| 生物| 历史| 道法 |
| 小学: 语文| 数学| 英语| 道德与法制| 科学| 试题: 小学| 初中| 中考| 高中| 高考| 作文: 小学| 初中| 高中| 满分| 技巧|素材|英汉词典 |
| 高校: 985/211| 各省市| 港澳台| 国外| 排名| 中考专辑| 高考专辑| 各省中学| 职业考试: 从业资格| 技术技能| 艺术等级| 公务员| 百年党史 |
| 课外: 教育动态| 教育法规| 老师榜| 家长帮| 学生派| 安全说| 古诗古文| 世界名著| 近代文学| 寓言故事| 格言名句| 阅读技巧| 在线许愿祝福 |
 移动版
移动版