【初中化学】人教版九年级下册 第十单元 酸和碱
 2022-01-10
2022-01-10 
 iXueHai.cn
iXueHai.cn
 爱学海
字体 - 小
+ 大 纠错指正
爱学海
字体 - 小
+ 大 纠错指正
|
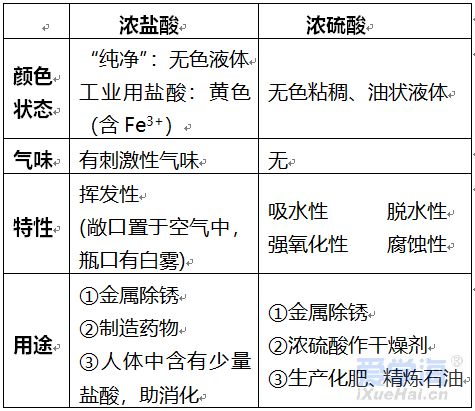
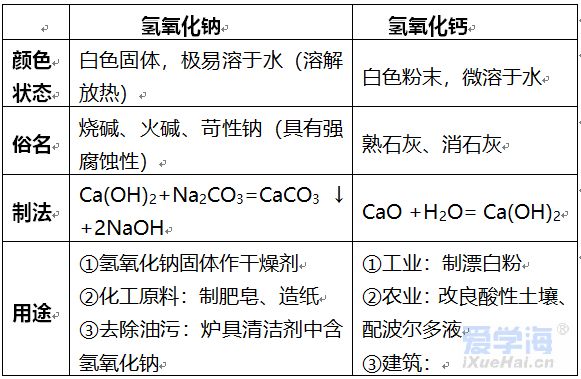
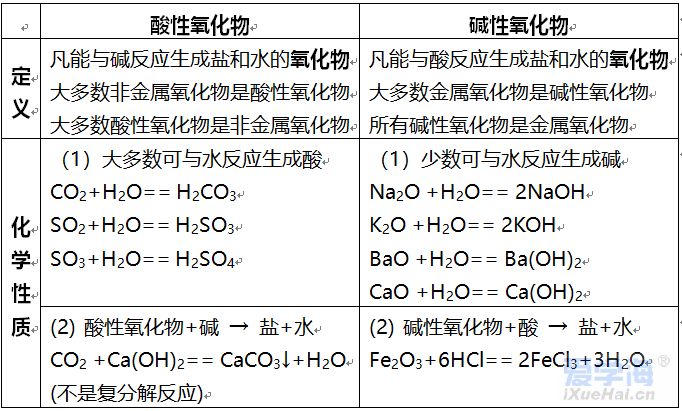
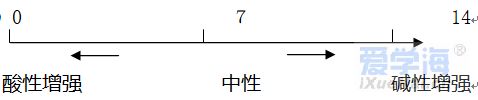
第十单元 酸和碱 一、酸、碱、盐的组成 (1)酸是由氢元素和酸根组成的化合物 如:硫酸(H2SO4)、盐酸(HCl)、硝酸(HNO3) (2)碱是由金属元素和氢氧根组成的化合物 如:氢氧化钠、氢氧化钙、氨水(NH3·H2O) (3)盐是由金属元素元素(或铵根)和酸根组成的化合物 如:氯化钠、碳酸钠 (4)酸、碱、盐的水溶液可以导电(原因:溶于水时离解形成自由移动的阴、阳离子) 二、酸 1、浓盐酸、浓硫酸的物理性质、特性、用途 2、酸的通性(具有通性的原因:酸离解时所生成的阳离子全部是H+) (1)与酸碱指示剂的反应: 使紫色石蕊试液变红色,不能使无色酚酞试液变色 (2)金属 + 酸 → 盐 + 氢气 (3)碱性氧化物 + 酸 → 盐 + 水 (4)碱 + 酸 → 盐 + 水 (5)盐 + 酸 → 另一种盐 + 另一种酸(产物符合复分解条件) 3、三种离子的检验 三、碱 1、氢氧化钠、氢氧化钙的物理性质、用途 2、碱的通性(具有通性的原因:离解时所生成的阴离子全部是OH-) (1)碱溶液与酸碱指示剂的反应: 使紫色石蕊试液变蓝色,使无色酚酞试液变红色(2)酸性氧化物+碱 → 盐+水 (3)酸+碱 → 盐+水 (4)盐+碱 → 另一种盐+另一种碱(反应物均可溶,产物符合复分解条件) 注:①难溶性碱受热易分解(不属于碱的通性) 如Cu(OH)2 ΔCuO +H2O 2Fe(OH)3 ΔFe2O3+3H2O ②常见沉淀:AgCl↓ BaSO4↓ Cu(OH)2↓ F e(OH)3↓ Mg(OH)2↓ BaCO3↓ CaCO3↓ ③复分解反应的条件:当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。 四、酸性氧化物与碱性氧化物 五、中和反应 溶液酸碱度的表示法——pH 1、定义:酸与碱作用生成盐和水的反应 2、应用: (1)改变土壤的酸碱性 (2)处理工厂的废水 (3)用于医药 3、溶液酸碱度的表示法——pH (1)图示:中间7位中性,高于7碱性增强,低于7酸性增强 (2)pH的测定:最简单的方法是使用pH试纸 用玻璃棒(或滴管)蘸取待测试液少许,滴在pH试纸上,显色后与标准比色卡对照,读出溶液的pH(读数为整数) (3)酸雨:正常雨水的pH约为5.6(因为溶有CO2) pH<5.6的雨水为酸雨。 |
| 高三: 语文| 数学| 英语| 物理| 化学| 地理| 生物| 历史| 思想政治| 信息技术| 初三: 语文| 数学| 英语| 物理| 化学| 历史| 道德与法制 |
| 高二: 语文| 数学| 英语| 物理| 化学| 地理| 生物| 历史| 思想政治| 信息技术| 初二: 语文| 数学| 英语| 物理| 地理| 生物| 历史| 道法 |
| 高一: 语文| 数学| 英语| 物理| 化学| 地理| 生物| 历史| 思想政治| 信息技术| 初一: 语文| 数学| 英语| 物理| 地理| 生物| 历史| 道法 |
| 小学: 语文| 数学| 英语| 道德与法制| 科学| 试题: 小学| 初中| 中考| 高中| 高考| 作文: 小学| 初中| 高中| 满分| 技巧|素材|英汉词典 |
| 高校: 985/211| 各省市| 港澳台| 国外| 排名| 中考专辑| 高考专辑| 各省中学| 职业考试: 从业资格| 技术技能| 艺术等级| 公务员| 百年党史 |
| 课外: 教育动态| 教育法规| 老师榜| 家长帮| 学生派| 安全说| 古诗古文| 世界名著| 近代文学| 寓言故事| 格言名句| 阅读技巧| 在线许愿祝福 |
 移动版
移动版