【高中化学】必修二第二单元 微粒之间的相互作用
 2021-10-01
2021-10-01 
 iXueHai.cn
iXueHai.cn
 爱学海
字体 - 小
+ 大 纠错指正
爱学海
字体 - 小
+ 大 纠错指正
|
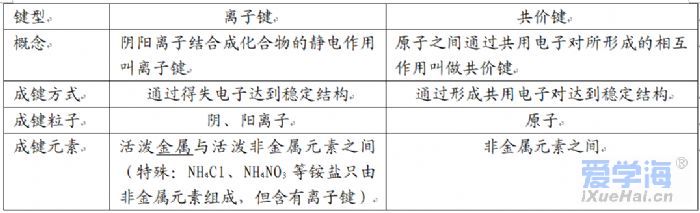
第二单元 微粒之间的相互作用 化学键是直接相邻两个或多个原子或离子间强烈的相互作用。 1.离子键与共价键的比较 离子化合物:由离子键构成的化合物叫做离子化合物。(一定有离子键,可能有共价键)
用电子式表示离子键形成的物质的结构与表示共价键形成的物质的结构的不同点:(1)电荷:用电子式表示离子键形成的物质的结构需标出阳离子和阴离子的电荷;而表示共价键形成的物质的结构不能标电荷。(2)[ ](方括号):离子键形成的物质中的阴离子需用方括号括起来,而共价键形成的物质中不能用方括号。 3、分子间作用力定义把分子聚集在一起的作用力。由分子构成的物质,分子间作用力是影响物质的熔沸点和 溶解性 的重要因素之一。 4、水具有特殊的物理性质是由于水分子中存在一种被称为氢键的分子间作用力。水分子间的 氢键 ,是一个水分子中的氢原子与另一个水分子中的氧原子间所形成的分子间作用力,这种作用力使得水分子间作用力增加,因此水具有较高的 熔沸点。其他一些能形成氢键的分子有 HF H2O NH3 。  |
本栏目热门阅读
- 【高中化学】高一 专题四 化学科学与人类文明
- 【高中化学】高一 专题三有机化合物的获得与应用 二、食品中的有..
- 【高中化学】高一 专题三 有机化合物的获得与应用 一、 烃
- 【高中化学】高一必修二 专题二 第二单元 化学反应中的热量
- 【高中化学】高一必修二 专题二 第四单元 太阳能、生物质能和氢..
- 【高中化学】高一必修二 专题二 第一单元 化学反应的速率与反应..
- 【高中化学】高一必修二 专题二 第三单元 化学能与电能的转化
- 【高中化学】高一必修二 第三单元 从微观结构看物质的多样性
- 【高中化学】必修二第一单元 原子核外电子排布与元素周期律
- 【高中化学】必修一 第四章 非金属及其化合物 习题
本栏目最新文章
| 高三: 语文| 数学| 英语| 物理| 化学| 地理| 生物| 历史| 思想政治| 信息技术| 初三: 语文| 数学| 英语| 物理| 化学| 历史| 道德与法制 |
| 高二: 语文| 数学| 英语| 物理| 化学| 地理| 生物| 历史| 思想政治| 信息技术| 初二: 语文| 数学| 英语| 物理| 地理| 生物| 历史| 道法 |
| 高一: 语文| 数学| 英语| 物理| 化学| 地理| 生物| 历史| 思想政治| 信息技术| 初一: 语文| 数学| 英语| 物理| 地理| 生物| 历史| 道法 |
| 小学: 语文| 数学| 英语| 道德与法制| 科学| 试题: 小学| 初中| 中考| 高中| 高考| 作文: 小学| 初中| 高中| 满分| 技巧|素材|英汉词典 |
| 高校: 985/211| 各省市| 港澳台| 国外| 排名| 中考专辑| 高考专辑| 各省中学| 职业考试: 从业资格| 技术技能| 艺术等级| 公务员| 百年党史 |
| 课外: 教育动态| 教育法规| 老师榜| 家长帮| 学生派| 安全说| 古诗古文| 世界名著| 近代文学| 寓言故事| 格言名句| 阅读技巧| 在线许愿祝福 |
Copyright © 2019-2023 爱学海 ixuehai.cn 版权所有 | 关于爱学海 | 商标证书 | 投诉反馈 | 版权声明 | 公司简介 | 中采网 | 粤ICP备09029428号
 移动版
移动版